¿CÓMO SE FORMA LA MATERIA? TIPOS DE ENLACES QUÍMICOS
 |
| Ilustración 1. Types of chemical Bond. -Wirdou. [1] |
El concepto de enlace es muy importante en Química, ya que a partir de los distintos tipos de enlace resultan las diferentes clases de sustancias con sus respectivas propiedades características.
Para comprender el concepto de enlace químico y sus diferentes tipos hay que tener claro lo que es un átomo y su comportamiento. Un átomo esta constituido por un núcleo formado por protones con carga positiva y neutrones sin carga y por otra parte, orbitando alrededor del núcleo se encuentran los electrones, estos tienen carga negativa. Al tener cargas opuestas, estas dos partes del átomo se atraen. Sin embargo, los electrones también se ven atraídos por los núcleos de otros átomos.
 |
| Ilustración 2. Atracción electroestática. [2] |
Así el enlace químico, se define como la fuerza responsable de la unión estable que existe entre dos átomos, con el fín de formar una molécula.
En la formación de un enlace los elementos que participan en él, tienden a rodearse de 8 electrones en su capa de valencia, siendo así más estables. Esto se conoce como "Regla del octeto". Para ello ceden, ganan o comparten electrones. La capa de valencia es el nivel de energía mas externo del átomo, en él se encuentran aquellos electrones que participan en el enlace.
Mientras los químicos creían que los átomos eran esferas rígidas fue posible admitir que cada átomo tuviera algo parecido a uno o más “ganchos o corchetes” que les permitieran unirse a otros átomos para formar las moléculas. [19] , [18].
Más tarde, en 1877 Thomson descubre el electrón y se llega a la conclusión de que los electrones son esos “ganchitos,”, es decir, son los intermediarios en el enlace químico.
Así se estableció la primera teoría de enlace químico, el enlace iónico.
 |
| Ilustración 5. Enlace iónico. -Wirdou. [5] |
Un enlace iónico es aquel tipo de unión química que se produce entre elementos metales y no metales con distinta electronegatividad, es decir, con distinta capacidad para atraer electrones. En este tipo de enlace químico un átomo de un elemento metálico transfiere un electrón a un átomo de un elemento no metálico. [21]
 |
Ilustración 6.b. Atracción. [6] |
 |
Ilustración 6.c. Enlace iónico. [6] |
Entre estos compuestos se cuentan especialmente las sales, un ejemplo; el cloruro de sodio, NaCl.
 |
| Ilustración 7. Estructura de la sal cloruro de sodio. [7] |
- Presentan elevados puntos de fusión y ebullición, por ello son sólidos a temperatura ambiente.
 |
| Ilustración 8. Sal. [8] |
- No son buenas conductores de la electricidad en estado sólido, ya que sus cargas están fijas en la red cristalina, pero sí lo hacen en disolución o fundidos debido a que en estos casos los iones si se pueden mover.
 |
| Ilustración 9. Conductividad sal. [9] |
- Son duros, al ser fuerte la atracción entre iones, y frágiles, debido a las repulsiones que aparecen al desplazarse una capa sobre otra, como podemos observar en la siguiente imagen.
 |
| Ilustración 10. Rotura sal. [10] |
 |
| Ilustración 13. Diamante. [13] |
- Puntos de fusión y ebullición bajos.
- No conducen la electricidad ni el calor.
- Tienen altos puntos de fusión y ebullición, pues los átomos están unidos por enlaces covalentes muy fuertes.
- No conducen el calor ni la electricidad, a excepción del grafito.
El último tipo de enlace químico que trataremos es el enlace metálico [20], este surgió al no poderse aplicar la teoría del enlace iónico ni covalente a los metales. Esta teoría también es conocida como teoría del electrón libre o del mar de electrones.
La red cristalina metálica está formada por iones de un metal, es decir átomos que han cedido sus electrones de valencia. Estos electrones están desubicados en el cristal y disponen de libertad de movimiento, son compartidos por todos los iones; constituyen la nube electrónica.
Las principales propiedades de los Cristales metálicos son:
- Son sólidos a temperatura ambiente. A excepción del mercurio que es un liquido a temperatura ambiente.
 |
| Ilustración 16. Mercurio. [16] |
- Sus temperaturas de fusión y ebullición son altas, de manera que el enlace entre los átomos es muy fuerte.
- Son Buenos conductores del calor y la electricidad.
- Presentan ductilidad y maleabilidad, debido a que las capas de iones se pueden deslizar unas sobre otras sin que se rompa la red metálica.
- Poseen un brillo metálico característico.
 |
| Ilustración 17. Pirita brillo metálico. [17] |
- [1] Ilustración 1. Types of chemical Bond. -Wirdou. https://wirdou.com/tag/chemical-bonds/ Fecha de acceso: 27/11/2021
- [2] Ilustración 2. Atracción electroestática. https://www.significados.com/ley-de-coulomb/ Fecha de acceso:27/11/2021
- [3] Ilustración 3. Capa de valencia. https://www.researchgate.net/figure/Electrones-de-valencia-de-un-atomo-de-silicio_fig2_267211218 Fecha de acceso: 27/11/2021
- [4] Ilustración 4. ¿De donde viene el concepto de enlace químico? Lucía Ferrer Biechy y Elisabet Fuentes Lara. Fecha de edición: 24/11/2021
- [5] Ilustración 5. Enlace iónico. -Wirdou. https://scenio.es/la-quimica-del-amor-sodio-cloro Fecha de acceso: 27/11/2021
- [6] Ilustración 6. (6a, 6b, 6c). https://www.significados.com/enlace-ionico/ Fecha de acceso: 27/11/2021
- [7] Ilustración 7. Estructura de la sal cloruro de sodio. https://concepto.de/enlace-ionico/ Fecha de acceso: 27/11/2021
- [8] Ilustración 8. Sal. https://menudospuntocero.com/15-tipos-de-sal-para-dar-variedad-a-nuestros-platos/ Fecha de acceso: 27/11/2021
- [9] Ilustración 9. Conductividad sal. https://slidetodoc.com/bases-de-qumica-general-trminos-importantes-materia-todo/ Fecha de acceso: 27/11/2021
- [10] Ilustración 10. Rotura sal. https://med.se-todo.com/himiya/19724/index.html?page=3 Fecha de acceso: 27/11/2021
- [11] Ilustración 11. Enlace covalente. https://www.redbubble.com/es/i/poster/Compartir-es-cuidar-Enlace-covalente-de-qu%C3%ADmica-de-NeXore/50395075.LVTDI Fecha de acceso: 27/11/2021
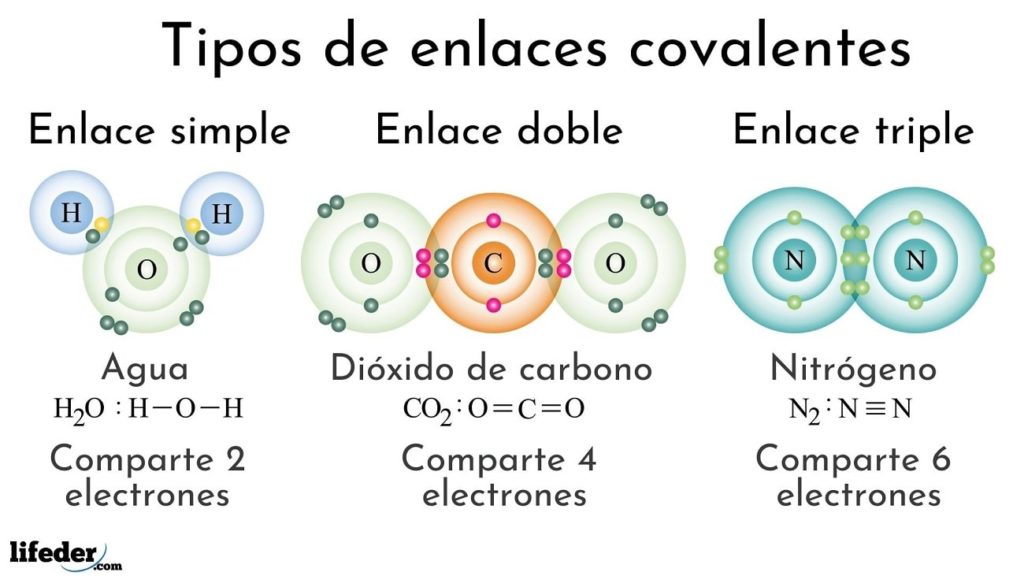
- [12] Ilustración 12. Tipos de enlace covalente. https://www.lifeder.com/enlace-covalente/ Fecha de acceso: 27/11/2021
- [13] Ilustración 13. Diamante. https://www.bbc.com/mundo/noticias-44946602 Fecha de acceso: 27/11/2021
- [14] Ilustración 14. Estructura dióxido de carbono. https://free3d.com/es/modelo-3d/carbon-dioxide-3d-model-co2-9947.html Fecha de acceso: 27/11/2021
- [15] Ilustración 15. Grafito y lápiz con mina de grafito. https://es.123rf.com/photo_13230470_pieza-en-bruto-de-mineral-de-carbono-roca-en-forma-de-grafito-una-forma-alotr%C3%B3pica-de-carbono-conocido-.html Fecha de acceso: 27/11/2021
- [16] Ilustración 16. Mercurio. https://mejorconsalud.as.com/el-veneno-del-mercurio-para-la-salud/ Fecha de acceso: 27/11/2021
- [17] Ilustración 17. Pirita brillo metálico. https://m.facebook.com/greenfields.minerals/photos/a.1192357444138108/1482717701768746/?type=3 Fecha de acceso: 27/11/2021
- Guadiel-grupo Edebé/ Química Bachillerato/ Guadiel 2003
- [18] https://ruidera.uclm.es/xmlui/bitstream/handle/10578/16459/TESIS%20Gonz%C3%A1lez%20Felipe.pdf?sequence=1&isAllowed=y Fecha de acceso: 27/11/2021
- [19] http://platea.pntic.mec.es/~jrodri5/web_enlaces_quimicos/antecedentes.htm Fecha de acceso: 27/11/2021
- [20]https://fisquiweb.es/Apuntes/Apuntes2Qui/EnlaceMetalico.pdf Fecha de acceso: 27/11/2021
- [21]https://www.todamateria.com/enlace-ionico/ Fecha de acceso: 27/11/2021
- [22] http://recursostic.educacion.es/newton/web/materiales_didacticos/enlacequimico/enlace/propiedadesionico.html?2&2 Fecha de acceso: 27/11/2021






No hay comentarios:
Publicar un comentario